J Nanobiotechnology:杂交细胞膜包被ICG脂质体可对浸润性胶质母细胞瘤边缘进行靶向血脑屏障穿透和精确成像
来源:生物谷原创 2024-10-22 11:09
本研究证明了杂交细胞膜涂覆ICG脂质体(hm - lipog -ICG)的成功开发,可用于靶向血脑屏障渗透和浸润性GBM边缘的精确成像。
胶质母细胞瘤(GBM)是一种原发性脑肿瘤,其特点是恶性程度和复发率异常高,且预后不良。尽管有多种治疗方式,手术切除仍然是目前最有效的治疗策略。在手术切除过程中,由于难以区分隐匿性肿瘤和健康组织的边界,常常导致手术切除不完全和手术效率低下。实现肿瘤最大切除对GBM生存的重要性强调了对浸润性肿瘤边缘清晰识别和可视化的迫切需要。
目前,术中光学技术已成为检测和定位GBM侵袭边缘的有前途的方法。特别是,荧光团吲哚菁绿(ICG)在近红外(NIR)窗口中具有荧光成像的优势,可以可视化肿瘤边缘。然而,ICG面临着血脑屏障(BBB)渗透效率低、肿瘤靶向性有限、循环系统半衰期短等挑战,这限制了其在GBM肿瘤边缘精确可视化中的适用性。
脂质体作为临床使用的给药系统,具有提高ICG稳定性和延长体循环半衰期的作用。此外,脂质体封装的ICG (lipo质体-ICG)不仅维持了ICG的代谢途径,而且在临床实践中具有潜在的应用前景。脂质体ICG天生具有通过增强渗透性和滞留性(EPR)效应被动靶向肿瘤区域的能力,因此在肿瘤部位表现出增强ICG积累的能力。此外,脂质体的双层分子膜结构提供了与细胞膜自发融合的前景。这些特性赋予脂质体天然的生物学功能和靶向能力,但它们也存在时间胶体稳定性有限、释放不受控制以及需要定制合成磷脂的问题。
Zhang等人提出的仿生方法的出现,推动了细胞膜伪装纳米颗粒在各种肿瘤模型中的应用,提高了GBM的诊断和治疗。基于癌细胞膜的仿生纳米探针表现出特殊的同型结合、血脑屏障渗透和免疫逃逸功能。然而,肿瘤特性固有的复杂性使得单型细胞膜不足以满足生物医学应用的多样化和严格要求。新兴的杂交细胞膜(HM)涂层方法为解决这些特定应用铺平了道路,从两种来源的细胞膜获得功能,这种独特的设计不仅保留了纳米颗粒的物理化学特征,而且还实现了同型靶向,并具有出色的长期循环性能。
针对特定癌细胞类型的研究表明,由于其向大脑的高转移能力,它们具有穿越血脑屏障的潜力。理论上,精心设计的HM有望同时利用来自组成细胞膜的两种生物功能——血脑屏障穿透和GBM靶向。这种定制的双功能脂质体探针,用融合细胞膜修饰,具有精确可视化GBM浸润边缘的潜力。

近日,来自暨南大学附属广东省第二总医院的研究者们在J Nanobiotechnology杂志上发表了题为“Targeted blood-brain barrier penetration and precise imaging of infiltrative glioblastoma margins using hybrid cell membrane-coated ICG liposomes”的文章,该研究证明了杂交细胞膜涂覆ICG脂质体(hm - lipog -ICG)的成功开发,可用于靶向血脑屏障渗透和浸润性GBM边缘的精确成像,强调了杂交细胞膜包被脂质体探针在精确观察和治疗浸润性GBM边缘方面的潜力。
手术切除仍然是胶质母细胞瘤(GBM)的主要治疗方式;然而,GBM边缘的浸润性使完全切除肿瘤变得复杂。此外,血脑屏障(BBB)对有效的探针递送构成了巨大的挑战,从而阻碍了精确的成像引导手术。
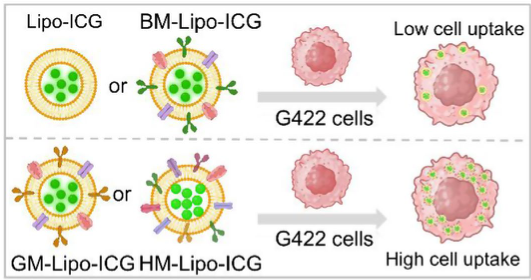
G422胶质瘤细胞摄取脂质icg、bm -脂质icg、gm -脂质icg和hm -脂质icg的示意图
图片来源:https://doi.org/10.1186/s12951-024-02870-1
在本研究中,研究者引入杂交细胞膜包被吲哚菁绿(ICG)脂质体(lm -脂质体-ICG)作为仿生近红外(NIR)荧光探针,用于靶向血脑屏障穿透和准确描绘浸润性GBM边缘。hm - lipoo -ICG在其核心内封装临床批准的ICG,并利用杂交细胞膜外部,实现特异性靶向和增强血脑屏障渗透。定量评估表明,HM-LipoICG的血脑屏障穿透效率是常规ICG脂质体的2.8倍。机制上,CD44受体介导的内吞作用促进了hm - lipop - icg的血脑屏障易位。此外,hm - lipop -ICG可实现高对比度近红外成像,在原位胶质瘤小鼠模型的GBM区域实现6.5的信本比,从而将肿瘤边缘检测准确率提高四倍(84.4%对22.7%)。hm - lipoo - icg的应用促进了荧光引导的精确手术,实现了GBM细胞的完全切除。
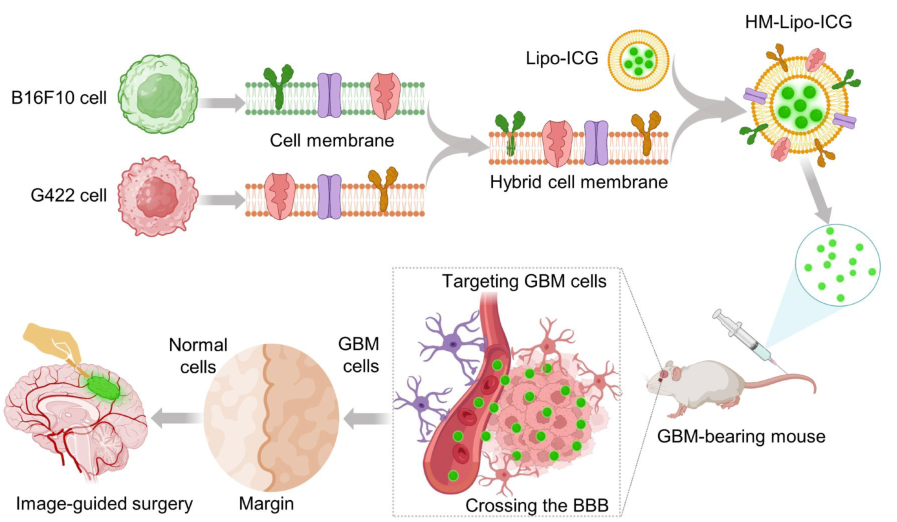
hm - lipoo - icg的制备过程及其在gbm荷瘤小鼠近红外荧光成像中的应用,包括肿瘤边缘描绘和指导手术切除
图片来源:https://doi.org/10.1186/s12951-024-02870-1
综上所述,本研究证明了杂交细胞膜涂覆ICG脂质体(hm - lipog -ICG)的成功开发,可用于靶向血脑屏障渗透和浸润性GBM边缘的精确成像。HM-LipoICG通过CD44受体介导的内吞作用和同型靶向,实现了优越的血脑屏障穿越和肿瘤靶向,显著提高了荧光引导下手术切除的准确性。hm - lipoo - icg表现出显著的稳定性、生物相容性和安全性,使其成为改善GBM手术结果的有希望的工具,这种仿生方法为浸润性肿瘤的精确可视化和完全切除提供了一种新的策略,有可能减少术后复发并延长患者的生存期。(生物谷 Bioon.com)
参考文献
Ping Liu et al. Targeted blood-brain barrier penetration and precise imaging of infiltrative glioblastoma margins using hybrid cell membrane-coated ICG liposomes. J Nanobiotechnology. 2024 Oct 5;22(1):603. doi: 10.1186/s12951-024-02870-1.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


